 이미지 확대보기
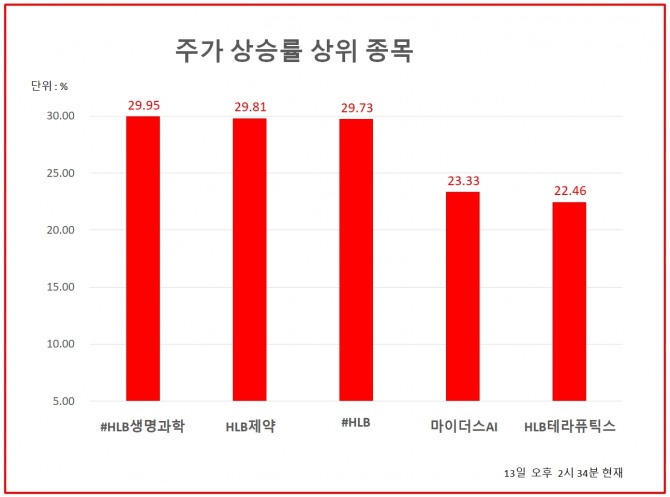
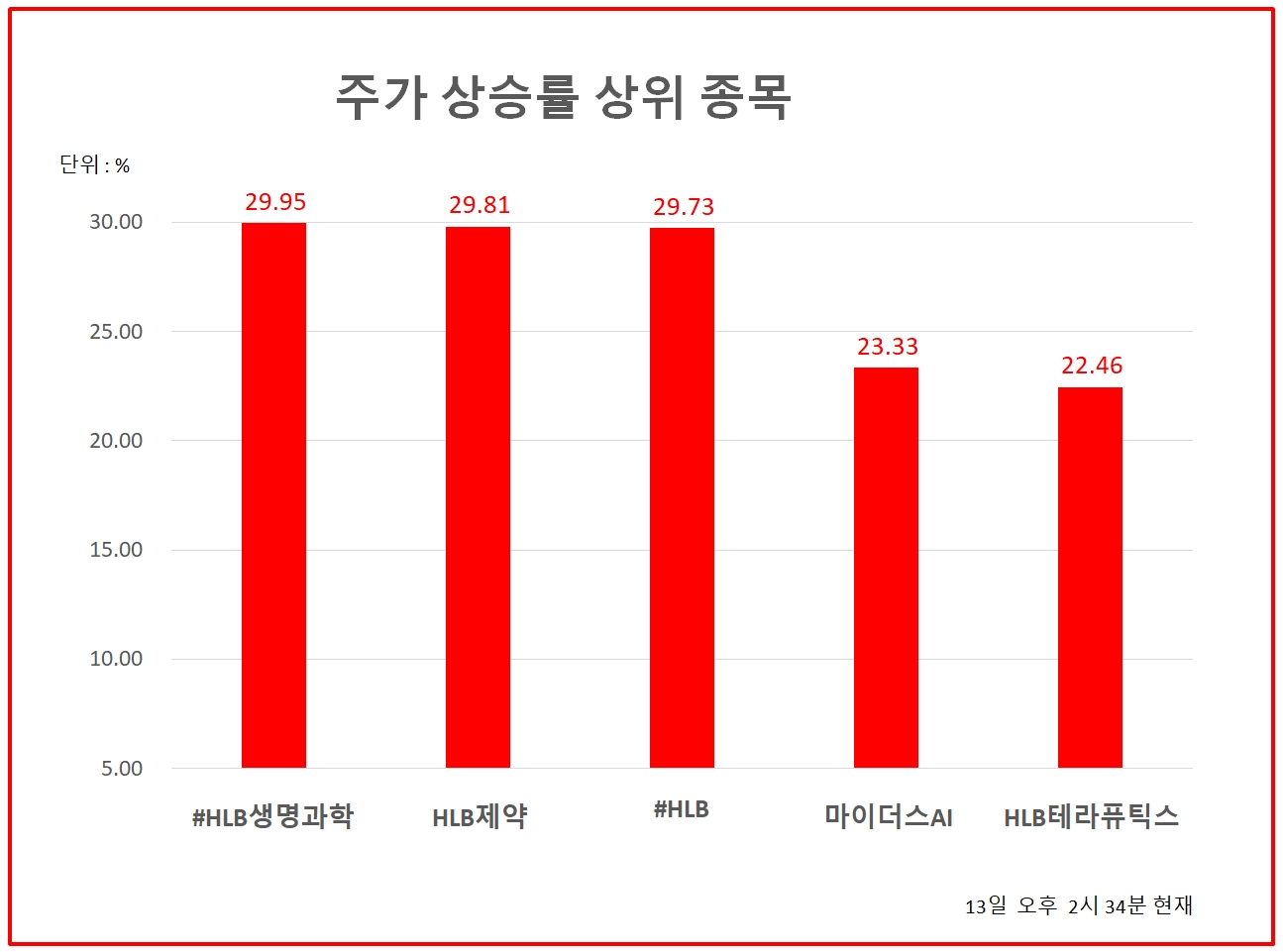
이미지 확대보기13일 한국거래소에 따르면 이날 HLB,HLB생명과학,HLB제약은 일제히 상한가를 기록중이다.
이에 따라 에이치엘비(HLB)가 항암치료제 '리보세라닙'의 글로벌 상용화에 한 발짝 더 다가섰다.
에이치엘비가 2009년 리보세라닙에 최초 투자를 단행한 이후 약 13년 만에 이룬 쾌거다.
지난 2019년 4월 시작된 간암 임상 3상은 한국과 미국, 중국을 비롯해 전 세계 13개 국가에서 543명의 환자를 대상으로 진행됐다.
암의 신생혈관생성을 억제(VEFGR-2 저해)하는 표적항암제 리보세라닙과 면역항암제 캄렐리주맙(PD-1 저해)을 병용투여한 이번 임상은 전체생존기간(OS)과 무진행생존기간(PFS)을 1차 유효성 지표로 설정해 간암 1차 표준치료제인 '소라페닙'(상품명 넥사바)과 대조하는 방식으로 진행됐다. 전체 데이터는 규정에 따라 세계적 권위의 암학회에서 공개될 예정이다.
핵심 지표인 OS, PFS의 통계적 유의성이 모두 확보됨에 따라 에이치엘비의 행보도 가팔라졌다.
이번 유효성 확보가 의미가 있는 것은 간암 시장은 환자 평균 생존율이 35%에 불과해 혁신 신약에 대한 미충족 수요가 매우 높은 분야라는 점에 기인한다.
최근 면역항암제가 치료제로 각광받고 있으나 면역항암제는 환자 반응률이 20% 수준에 불과해 다국적 제약사들을 중심으로 이를 극복하기 위한 병용임상이 활발히 진행되고 있다. 하지만 병용요법 치료를 위해서는 두 약물의 항암효과는 물론, 낮은 부작용도 입증돼야 한다.
이 가운데 리보세라닙은 암이 산소와 영양분을 공급받기 위해 생성하는 신생혈관의 성장인자(VEGFR-2)를 차단해 암세포의 성장과 전이를 효과적으로 막는다. 즉 리보세라닙은 다양한 암종에 적용이 가능하며, 부작용이 적어 다른 항암제와의 병용성도 탁월한 최적의 병용 파트너라는 얘기다.
에이치엘비 관계자는 "간암은 전 세계적으로 6번째 많이 발병하는 암으로 혁신 항암신약의 빠른 개발이 절실한 분야"라며 "당사는 말기 위암 NDA를 준비하며 리보세라닙에 대한 제조품질관리(CMC) 준비를 상당 부분 진행한 만큼 신약생산 인프라를 조속히 갖춰 FDA 신약승인을 받는 즉시 전 세계 환자들에게 빠르게 공급하겠다"고 말했다.
정준범 글로벌이코노믹 기자 jjbkey@g-enews.com
[알림] 본 기사는 투자판단의 참고용이며, 이를 근거로 한 투자손실에 대한 책임은 없습니다.
















![[초점] 인구 노령화 여파, 이젠 ‘75세’부터가 노인](https://nimage.g-enews.com/phpwas/restmb_setimgmake.php?w=184&h=118&m=1&simg=20240425095633009479a1f3094311109215171.jpg)