심각한 면역저하자의 코로나19 위중증 예방 기대
 이미지 확대보기
이미지 확대보기이는 질병관리청이 이달 10일 식약처에 이부실드의 긴급사용승인을 요청한 데 따른 것이다.
식약처는 코로나19 백신을 접종하기 어려운 환자에 대한 감염 예방 필요성, 안전성·효과성·품질에 대한 검토, 전문가 자문 등을 종합적으로 고려해 '공중보건 위기대응 의료제품 안전관리·공급위원회' 심의를 거쳐 긴급사용승인을 결정했다.
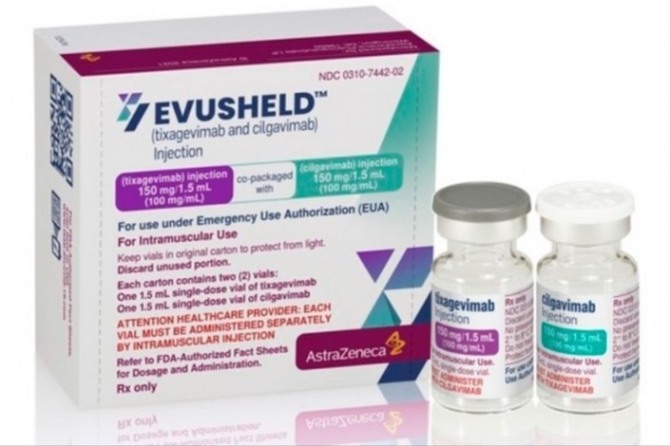
이부실드는 국내 최초로 도입되는 코로나19 예방용 항체의약품으로, 코로나19 바이러스 스파이크 단백질에 결합해 바이러스가 우리 몸속으로 침투하지 못하도록 중화하는 항체 복합제다.
한 상자에 포장된 '틱사게비맙'(150㎎) 1병과 '실가비맙'(150㎎) 1병을 서로 다른 근육 부위에 연속으로 주사하는 방식으로 투여한다.
투여 시 관찰된 부작용으로는 두통(6.6%), 피로(4.7%) 및 기침(3.5%) 등 경미한 이상반응이 대부분이다. 안전성에 대한 우려는 낮은 것으로 식약처는 판단했다.
식약처 관계자는 "이번 긴급사용승인 이후 이부실드를 사용하는 과정에서의 부작용 정보를 수집하고 국내외 안전성 정보를 지속해서 분석·평가하는 등 안전 사용 조치를 지속할 예정"이라고 말했다.
이도열 글로벌이코노믹 기자 bbh753@g-enews.com
























![[뉴욕증시 주간전망] 이란 전쟁·유가 흐름에 촉각...S&P500 20%...](https://nimage.g-enews.com/phpwas/restmb_setimgmake.php?w=80&h=60&m=1&simg=2026032205134908223be84d87674118221120199.jpg)
















