 이미지 확대보기
이미지 확대보기6일 셀트리온에 따르면 '램시마SC'제형은 환자가 병원을 찾아 2시간 이상 정맥 주사를 맞아야 기존 램시마에 비해 환자가 집에서 의약품을 보관하다가 사용 주기에 맞춰 투여하면 된다. 편의성 면에서 상당한 잇점이다.
유럽 시장에 진출하게 되면 IV제형의 바이오시밀러 '램시마'와 SC제형의 '램시마SC'를 양대축으로 삼아 유럽의 류머티즘관절염과 염증성장질환 치료제 시장을 겨냥하겠단 의도다.
또한 셀트리온은 대규모 임상시험 데이터를 인용해 자사 바이오시밀러가 의료진과 환자의 신뢰를 얻기 충분하단 입장이다.
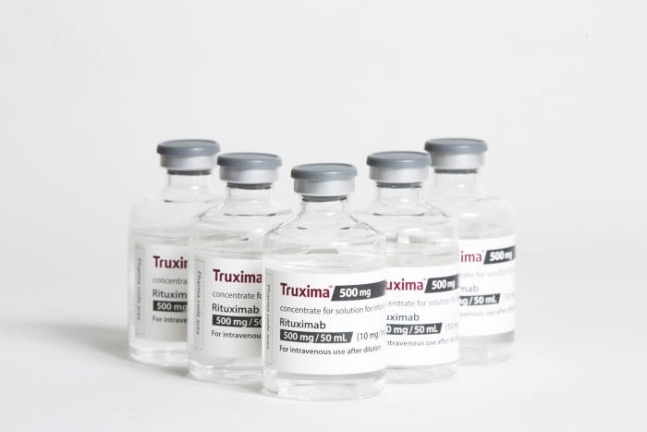
셀트리온은 앞서 지난 28일 미국 식품의약국(FDA)으로부터 트룩시마의 판매 허가를 받으면서 임상시험 데이터를 미국 혈액학회에서 발표하면서 시장 개척에 나섰다.
혈액암(AFL) 환자 140명에 트룩시마와 오리지널 의약품을 나눠 투여한 뒤 2년 동안의 경과를 비교·분석한 결과, 두 의약품의 전체 생존율과 치료반응 등이 유사했다.
셀트리온의 바이오시밀러가 큰 판매고를 올릴 것이란 전망에는 정부의 정책 때문이라는 지적도 있다. 바이오시밀러는 기존 바이오의약품보다 저렴해 이를 사용하면 정부의 건강재정 부담을 줄일 수 있다는 이유에서다.
셀트리온은 "램시마는 오리지널 약과 비교해 효과는 유사하면서도 가격은 40~45%가량 저렴해 보건의료재정 부담을 현저히 줄일 수 있다"며 "경미한 수준의 질병을 앓고 있다 하더라도 삶의 질 개선을 위해 효과적인 치료를 받아야 한다"고 지적했다.
한아름 기자 arhan@g-enews.com






























![[모바일 랭킹] 작혼, '블루 아카이브' 컬래버 후 매출 119위→11...](https://nimage.g-enews.com/phpwas/restmb_setimgmake.php?w=80&h=60&m=1&simg=2024042016003305766c5fa75ef8612254575.jpg)