구완성 연구원은 "지난 29일에서 31사이 미국 컨퍼런스에서 투자자들의 바이오시밀러에 대한 관심은 여전히 높았다"며 "오는 6월 추가 공장 실사 전 트룩시마 식품의약품(FDA)보완자료를 제출한 점이 긍정적"이라고 설명했다.
이어 "허쥬마의 보완자료는 6월중 제출할 예정이며 7~8월중 추가 실사를 통해 우려가 해소될 것"이라며 "11~12월 중 트룩시마와 허쥬마의 미국 허가가 가능할 것"으로 전망했다.
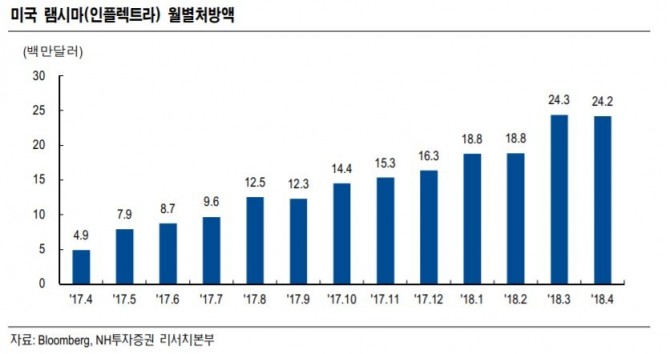
바이오시밀러 시장은 미국에서 인플렉트라(램시마)가 오리지널 대비 15% 인하된 가격(ASP 기준)으로 판매되고 있다. 유럽에서 출시되는 트룩시마, 허쥬마 등 초기 품목의 가격 인하율은 25%, 그 다음해 35%, 45% 등 단계적으로 인하했다. 제조원가가 낮고, 임상비용이 거의 들지 않으며, 경쟁자가 많은 합성 제네릭 시장과는 다른 market dynamics를 나타냈다.
구 연구원은 "셀트리온 헬스케어 기준 올해 연간 매출액은 1조5000억원이 전망된다"면서 "1조6000억원 규모의 재고자산은 큰 문제가 되지 않을 것"이라고 예상했다.
아울러 "최근 삼성바이오로직스 사태로 셀트리온의 연구개발(R&D)비용의 자산화 이슈를 혼돈하는 투자자들이 많지만 아직까지 금융감독워의 새로운 가이드라인 제시나 변화움직임이 없어서 기존 비용 처리 방식에서 큰 변화는 없을 것"으로 전망했다.
손현지 기자 hyunji@g-enews.com
[알림] 본 기사는 투자판단의 참고용이며, 이를 근거로 한 투자손실에 대한 책임은 없습니다.
































![[모닝픽] 삼성SDI, 시니어 테크와 6년간 배터리 분리막 구매 계약](https://nimage.g-enews.com/phpwas/restmb_setimgmake.php?w=80&h=60&m=1&simg=2024042005594605447e8b8a793f7210178127232.jpg)